مستقبل الرعاية الصحية الشخصية بين الحاجة إلى آليات جديدة لتعلم الآلة وتطوير طرق لتحليل البيانات الجينومية لكل خلية
الاثنين، 21 أكتوبر 2024

رغم أن ما نراه أو نستخدمه من أشياء لا يتحسن بالضرورة مع الوقت، إلا أن التكنولوجيات بحسب قانون مُور – الذي يُستشهد به كثيراً – تميل إلى أن تصبح أفضل وأرخص. ويشير هذا القانون إلى ما يصاحب تضاعف عدد الترانزستورات التي يمكن وضعها على دائرة متكاملة خلال قرابة العامين من تطور في قوة المعالجة والتأثير المحدود على التكلفة، ما يعتبر أمراً جيدً للعلوم وتطورها.
ويمكن القول إن مجال علم الأحياء، قد استفاد من تطورات مشابهة تخص التسلسل الجيني، وهي العملية التي بواسطتها يتم تحديد تسلسل الجزيئات التي تشفر المعلومات الجينية مثل الحمض النووي الريبوزي المنقوص الأكسيجين (DNA) والحمض النووي الريبوزي (RNA)؛ فعندما تمكن العلماء للمرة الأولى من استكمال تحديد تسلسل الجينوم البشري في عام 2003، وصلت تكلفة هذا المشروع إلى 3 مليارات دولار – في حين أن اليوم، يمكن إنجاز الأمر نفسه مقابل بضع مئات من الدولارات.
وعن هذا التطور يوضح د. إدواردو بلترامي أن: “أحد الأشياء المهمة التي حدثت خلال العقد الماضي هو أن عملية تحديد تسلسل الحمض النووي الريبوزي المنقوص الأكسيجين باتت سلعة بأسعار تنافسية أصبح العلماء معها قادرين على طرح المزيد من الأسئلة البحثية وإجراء تجارب على نطاق أوسع”، مضيفاً “إذا تمكنا اليوم من تصميم تجارب بيولوجية بحيث يمكن تحليل نتائجها من خلال تقنيات التسلسل، فسنتمكن من جمع بيانات هائلة”.
يذكر أن د. بلترامي التحق مؤخراً بقسم علم الأحياء الحاسوبي في جامعة محمد بن زايد للذكاء الاصطناعي، ويعمل على تطوير أساليب وآليات لتحليل الكم الهائل من البيانات التي ينتجها العلماء باستخدام تقنيات التسلسل الجيني التي أصبحت بأسعار في المتناول بشكل متزايد.
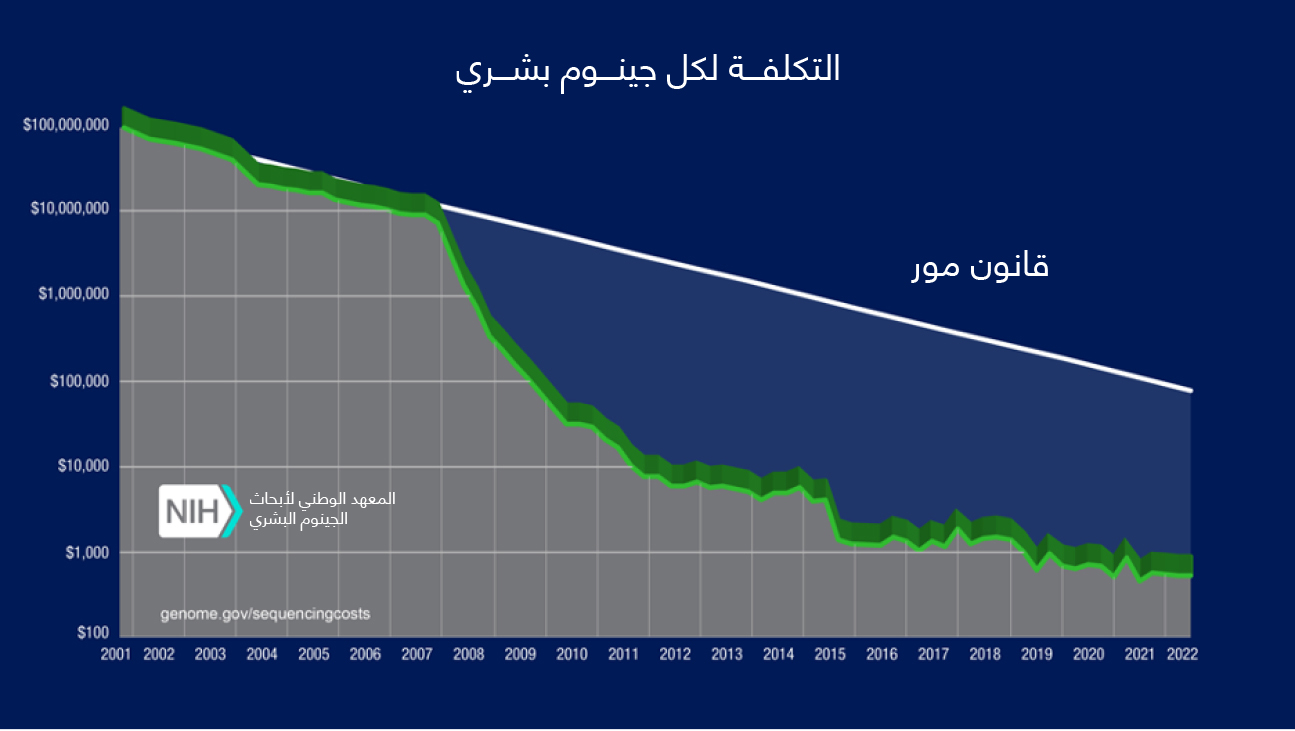
انخفاض تكلفة عملية تحديد تسلسل الجينوم البشري بشكل أسرع مما يتوقعه قانون مُور على مدى العقدين الماضيين. المصدر: Wetterstrand KA. DNA Sequencing Costs: Data from the NHGRI Genome Sequencing Program (GSP) متوفر على: www.genome.gov/sequencingcostsdata – تم زيارة الموقع بتاريخ 17 سبتمبر 2024.
الحمض النووي والحمض النووي الريبوزي والبروتينات
يشير تسلسل الجينوم إلى المعلومات الوراثية الموجودة في كائن حي ما؛ والمسؤولة عن تحديد كيفية تطوره ونموه وهرمه، لكن العلماء يمكنهم أيضاً تحديد تسلسل الحمض النووي الريبوزي المشتق من الحمض النووي الريبوزي المنقوص الأوكسيجين من خلال ما يعرف بعملية النسخ وتمثيل المعلومات عن النظم الجينية النشطة في الخلية. وبدورها الخلايا تستخدم الحمض النووي الريبوزي لصنع البروتينات من خلال عملية تُعرف باسم الترجمة.
ونظراً لأن الحمض النووي الريبوزي يحمل معلومات حول البروتينات التي تصنعها الخلايا والعمليات البيولوجية النشطة فيها، فإن قياس تركيز الحمض النووي الريبوزي مهم للغاية؛ ففي حين أن الحمض النووي الريبوزي المنقوص الأوكسيجين لكائن حي معين هو نفسه عموماً في جميع أنواع الخلايا في أوقات مختلفة، فإن الحمض النووي الريبوزي تختلف معدلاته وفقاً لنوع الخلية ويتغير باستمرار، ما يوفر معلومات عن التعبير الجيني.
وعن أهمية هذا الحمض النووي يقول د. بلترامي: “إذا كنت تريد أن تعلم ما تقوم به الخلية الآن، فأنت بحاجة إلى النظر إلى الحمض النووي الريبوزي”.
ويركز د. بلترامي في عمله مؤخرا على تقنية قوية تعرف باسم عملية تحديد تسلسل الحمض النووي الريبوزي للخلية الواحدة، وهي تقنية لقياس هذا الحمض داخل آلاف الخلايا المنفردة، مما يوفر قراءة دقيقة عن الحالة الجزيئية لكل خلية. ويشار، في هذا الصدد، إلى أن العلماء قاموا لسنوات بتحديد تسلسل الحمض النووي الريبوزي، غير أن المقاربات السابقة القائمة على التسلسل الكلي لهذا الحمض كانت تؤدي إلى نتائج غير دقيقة وتَغفَل عن الاختلافات والتعقيدات المهمة.

تحافظ تقنية تحديد تسلسل الحمض النووي الريبوزي للخلايا المنفردة على عدد جزيئات الحمض نفسه من كل نوع من أنواع الخلايا، مما يوفر تفاصيل أكبر تتعلق بكيفية التعبير عن الجينات في أنواع مختلفة من الخلايا – الصورة هي مساهمة من إدواردو بلترامي.
ويوضح د. بلترامي أنه إذا كانت عملية تحديد تسلسل الحمض النووي الريبوزي التقليدية شبيهة بشرب عصير من الفاكهة، فإن تحديده اعتماداً على المقاربة الفردية [أي لكل خلية على حدة]، فإن ذلك شبيه بتذوق التوت الأزرق؛ بالدقة العالية التي توفرها تقنية تحديد تسلسل الحمض النووي الريبوزي للخلية الواحدة، تعد مهمة خاص لدراسة الأسباب الكامنة وراء مرض ما، أو تحديد الأنواع الفرعية للمرض، حيث تلعب غالباً مجموعة صغيرة من الخلايا دوراً في مرض بعينه. ويشرح د. بلترامي هذا قائلاً: “في عينة من 10,000 خلية، قد يكون لديك 10 أو 20 خلية من نوع نادر من الخلايا تحدد عملية بيولوجية مهمة؛ وإذا قمت بعملية تحديد تسلسل الحمض النووي الريبوزي باعتماد المقاربة الكلية، فستغفل عن الأنواع النادرة من الخلايا”.
الرعاية الصحية الفردية
إضافة إلى تحسين فهمنا الأساسي للبيولوجيا، فإن دراسة الحمض النووي الريبوزي أو ما يُعرف بعلم تقنيات النسخ، لها آثار عملية على الطب والرعاية الصحية الفردية أو الشخصية، وهي مقاربة علاجية للأمراض تأخذ في الاعتبار التنوع البيولوجي والجزيئي الفردي للأشخاص.
وعن أهمية دراسة الحمض النووي الريبوزي، يوضح د. بلترامي أن شخصين قد يعانيان مما قد يبدو أنه المرض نفسه بناءً على الأعراض الملحوظة، ولكن الأسباب الجزيئية للأمراض قد تكون مختلفة. فمعظم الأمراض المناعية الذاتية – مثلا – هي عائلات من أمراض معقدة وأمراض فرعية بأعراض متشابهة، ولكن بميكانيزمات مختلفة تتسبب فيها. فمرض التهاب الأمعاء، على سبيل المثال، ليس مرضاً واحداً، بل هو مجموعة من الحالات الالتهابية، وأشهرها التهاب القولون التقرحي و’مرض كرون‘ – كل منهما له أسباب وآليات جزيئية وعلاجات مختلفة.
إن القدرة على القيام بإجراءات تشخيصية دقيقة، يُعدُّ أمراً محورياً لتطوير الطب الدقيق، وعملية تحديد تسلسل الحمض النووي الريبوزي للخلية الواحدة وما توفره من بيانات عالية الدقة تَعِد بالشيء الكثير للعلماء حيث ستمكنهم من تحصيل فهم أعمق وأدق عن أسباب مرض ما واختيار العلاجات الأكثر ملاءمة للبيولوجيا الفريدة للمريض.
ويعتقد د. بلترامي أننا في المستقبل سنستفيد من الفحوصات الدورية والغنية بالبيانات في شكل ما يطلق عليه اسم “التحاليل الجينومية الروتينية للخلايا المفردة”، والتي ستمكن الأشخاص من تحليل حالتهم الصحية في منازلهم. وسيكون باستطاعتهم إخضاع أنفسهم لهذه الاختبارات مرتين في اليوم – صباحاً ومساءً، لأن وظيفة الخلية تتأثر كثيراً بالإيقاع اليومي – والحصول على تقرير مفصل عن صحتهم العامة. وتختلف هذه الطريقة عن أسلوب التشخيص الحالي، حيث نادراً ما يتم إجراء تحاليل – مثل تحاليل الدم – التي تولد بيانات كثيرة، غير أنها لا تكشف عن الكثير من التفاصيل مثل مستويات السكر التي يمكن الحصول عليها باستخدام جهاز مثل جهاز مراقبة الجلوكوز.
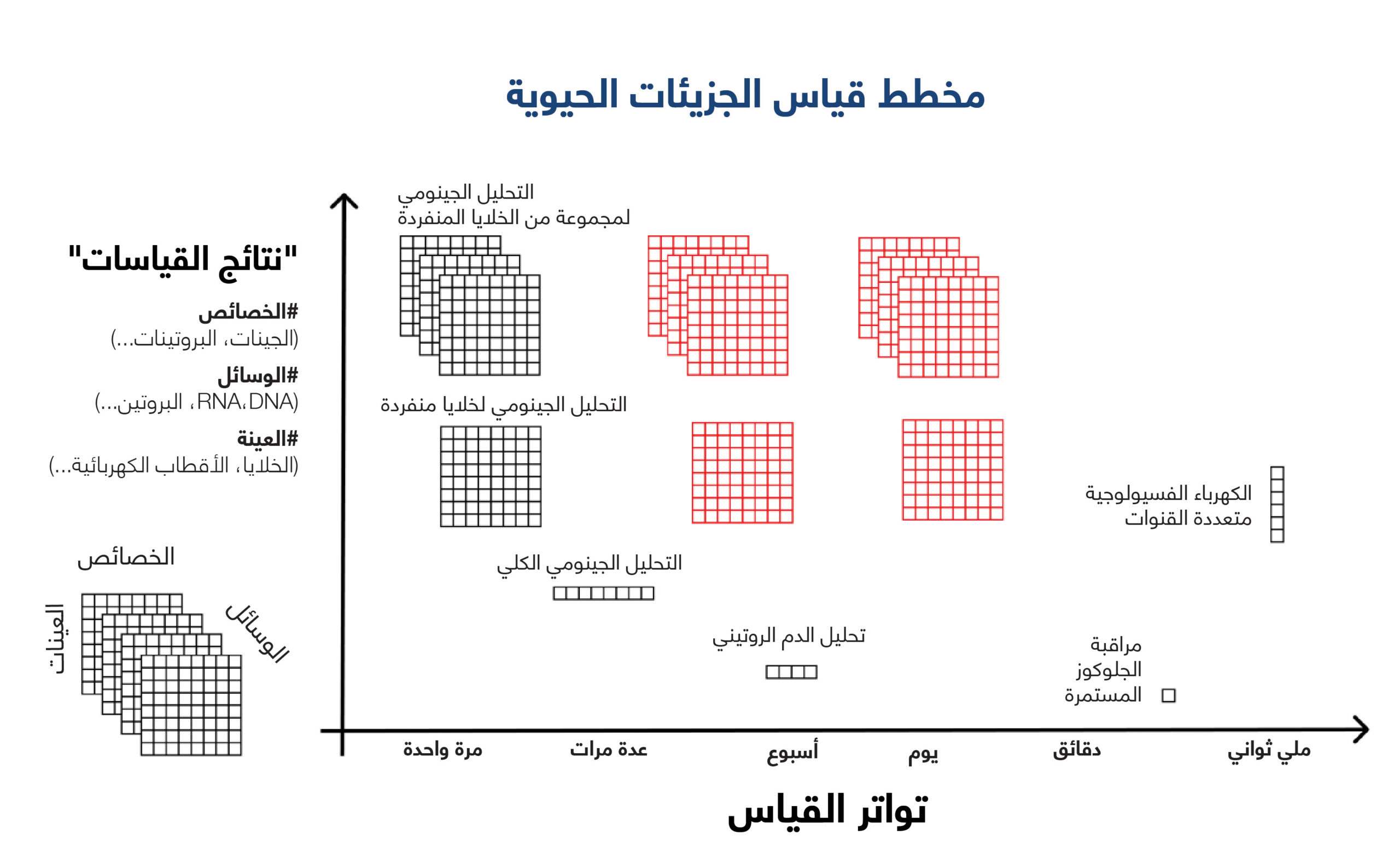
يرى د. بلترامي أن ’التحليلات الجينومية الروتينية لخلايا مفردة‘ و’التحليلات الجينومية لمجموعة من الخلايا ‘ (باللون الأحمر) ستصبح ممكنة مع استمرار انخفاض تكلفة عملية تحديد التسلسل الجيني – الصورة هي مساهمة من إدواردو بلترامي.
وعن هذه القياسات يضيف د. بلترامي: “ستصبح هذه التحليلات الطبية الغنية بالنتائج أرخص وأسهل للتنفيذ، وستمكننا من الحصول على بيانات أكثر بألف مرة مما لدينا حالياً، غير أنه وحتى ندعم بها خدمات رعاية صحية فردية، نحتاج إلى تطوير آليات يمكنها تحليل البيانات بكميات هائلة، وأعتقد أن تقنية تعلم الآلة هي الوحيدة القادرة على رفع هذا التحدي”.
عصر طبي جديد
أحد التحديات التي تواجه تطوير الآليات والأساليب لتحليل البيانات البيولوجية هو أنه من الصعب وضع اليد على “حقيقة أساسية” ضمن مجموعة البيانات الجزيئية.
وعن تعقيد تحليل البيانات البيولوجية يوضح د. بلترامي: “إنها ليست مثل صور لحيوانات يمكن تصنيفها باعتبارها صور لقطط وليست لكلاب”، مضيفاً “نظراً لأن علم الأحياء الجزيئي معقد للغاية، فليس لدينا صورة بديهية عنه، والتأكد من أننا في المسار الصحيح يتطلب الكثير من التعمق في الأدبيات البيولوجية التي تضمن أن النتائج التي لدينا حقيقية، وليست ضوضاء أو أخطاء تجريبية”.
ويعتقد د. بلترامي أن جامعة محمد بن زايد للذكاء الاصطناعي هي أفضل مكان للبحث في هذا المجال وتطوير أساليب وآليات جديدة لتحليل البيانات البيولوجية نظرا لما تتوفر عليه من خبراء وعلماء يشكلون “نخبة مختارة” ستتوسع بانضمام المزيد من الباحثين ذوي الخبرة في علم الأحياء ضمن قسم علم الأحياء الحاسوبي فيها.
ويرى د. بلترامي أن التحليل الجينومي الروتيني للخلايا المنفردة لديه القدرة على تحويل كيفية تشخيص الأمراض وعلاجها. وستساعد آليات جديدة لتعلم الآلة الباحثين على فك شفرة هذا الكم الهائل من البيانات البيولوجية وفهم العمليات الجزيئية التي تؤثر على صحة الفرد بشكل أفضل. كما سيتمكن الأطباء من تصميم العلاجات بناءً على علم الأحياء الفردي. وقد تعمل أيضاً هذه الابتكارات على تمكين الناس من التحكم بشكل أفضل في صحتهم من خلال الفهم المستمد من التشخيصات المتكررة والغنية بالبيانات، مما يمثل تحولاً عن التقارير الطبية العرضية. ولتحقيق هذه الرؤية ما يزال هناك الكثير من العمل الذي يجب القيام به.
وعن هذه الثورة القادمة يقول د. بلترامي: “ستحدث تقنيات التحليل الجينومي للخلايا المنفردة ثورة في الطب الشخصي. وسيكون بإمكاننا الحصول على تشخيص لكل شيء، بما في ذلك حالات الصحة العقلية مثل الاكتئاب والاضطراب ثنائي القطب، والتي نعتمد في تشخيصها اليوم على ملاحظات سلوك المرضى”.
- علم الأحياء الحاسوبي ,
- الطب ,
- علم الأحياء ,
- الجينوم ,
- العلاج ,
- الحصة ,
أخبار ذات صلة
إنجاز علمي يعيد تعريف فهم العلاقات السببية ويكشف ما تخفيه البيانات
كشف العلاقة السببية: دراسة حديثة تقدم خوارزمية متطورة لتحليل المتغيرات الكامنة وفهم العلاقات السببية المعقدة دون الاعتماد.....
- كشف العلاقة السببية ,
- ICLR ,
- البحوث ,
- المؤتمرات ,
- تعلّم الآلة ,
أداة جديدة لتحليل البيانات الطبية المشتركة لأكثر من مستشفى مع مراعاة الخصوصية
يُمكّن إطار جديد طوّره باحثون في جامعة محمد بن زايد للذكاء الاصطناعي المؤسسات من اكتشاف الأنماط المشتركة.....
- مجموعة البيانات ,
- إطار ,
- المؤتمر ,
- framework ,
- AISTATS ,
- البحث العلمي ,
- متعدد الوسائط ,
- تعلّم الآلة ,
ابتكار جديد يعيد صياغة معادلة تدريب النماذج اللغوية بكفاءة عالية
باحثون من جامعة محمد بن زايد للذكاء الاصطناعي، يطورون تقنية جديدة تساعد في الضبط الدقيق للنماذج اللغوية.....
- الضبط الدقيق ,
- ICLR ,
- الخوارزميات ,
- النماذج اللغوية ,
- المؤتمرات ,
- تعلّم الآلة ,


